醫療器械技術評審究竟是什么樣的呢?有人說醫療器械技術評審是審核資料那就太簡單了,那審核是不是符合標準太片面了;審核產品又不夠具體。那技術審評到底是什么呢?
?
?

?
?
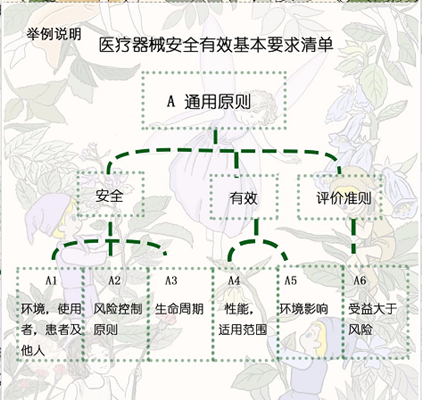
醫療器械技術評審是對擬上市醫療器械產品的安全有效性進行系統性評價的過程,這可能很抽象,要解釋好這兩個概念要從《醫療器械安全有效基本要求清單》和《醫療器械 風險管理對醫療器械的應用》(YY/T0316)說起。這是醫療器械注冊申報資料第三章和第八章的要求,這兩份文件在產品安全有效性系統性評價中起著非常關鍵的作用。正如《醫療器械 風險管理對醫療器械的應用》(YY/T0316)所定義的,安全性是免除于不可接受風險的能力。醫療器械是沒有絕對安全,所謂的安全是相對風險而言。
?
何為有效?
有效在字典的定義是“能實現預期用途”產品都是預期解決醫療的某個問題。如高頻電刀的預期用途為在外科手術中,用于軟組織的切割和凝血。那么實現軟組織切割和凝血的能力即為高頻電刀的有效性。
?
安全和有效之間的聯系又是什么?
正如前文所述醫療器械沒有絕對的安全,所謂的安全是相對風險而言,技術審評最終得出的結論是:基于醫療器械的有效性(受益)與醫療器械的安全性問題(風險)綜風險合之后是否能夠得出受益大于風險的結論。
?
隨著認知程度、教育程度、社會經濟、患者實際的和覺察的健康狀態以及其他因素的變化該接受準則也會不斷的變化和發展。在審評的初級階段,我們可能都知道有源醫療器械需要遞交YY0505-2012電磁兼容檢測報告,并對報告內容進行審評。
?
但這并不是完整的深度評價過程。完整的深度評價過程應包括按照《醫療器械安全有效基本要求清單》確定是否適用B52.3的相關要求、證明符合該要求的方法,最后對符合性的證據文件進行評價。醫療器械產品是否會對環境產生電磁干擾,如適用其所產生的電磁干擾應在可接受的范圍證明其產生的電磁干擾在可接受的范圍方法為YY0505-2012電磁發射部分內容證明符合性的客觀證據為YY055-2012標準的檢測報告并對檢測報告內容進行評價。而電磁干擾只是醫療器械產品應該考慮的風險之一,因此完整深度審評的同時還應對產品安全有效性進行廣度評價,例如還應考慮產品的電氣安全方面的風險、生物學方面的風險、能量相關的風險以及產品的有效性等。
?
如果清單中適用的條款完整,證明符合性采用的方法合理、恰當,所提交證據全面、合理、充分,則可認為產品符合安全有效基本要求,通過技術審評,行政審批,獲準注冊。
?
?
?
獲準注冊
正如我在解釋何為安全性時提到的,你會發現安全性和風險之間緊密聯系。醫療器械安全有效基本要求清單的內容則是由請人對按照風險控制原則在設計和生產過程中所形成文件的邏輯性梳理。清單中安全性相關的要求是各申請人在風險管理過程中識別出的安全特征通用總結和提煉,清單中的方法和客觀證據則是為了證明申請人風險控制措施的有效性,最終的審評結論則是基于產品的剩余風險和產品有效性的綜合考量。
?
因此掌握YY/T0316的風險管理思路,在審評過程中結合申請人提供的風險管理資料,對于我們完成產品安全有效性系統性評價至關重要。尤其是清單是基于通用原則制作而成,并不能夠保證窮舉所有產品的要求,風險管理的思路還能夠幫助我們提出更多安全性相關的問題以查漏補缺。
?
通過這樣的方法,所有的審評意見都有依據可尋。如果申請人能夠提供完整充分的安全有效清單和風險管理資料也會提高我們審評的效率和質量,技術審評的一致性、規范性、科學性、系統性也會大大提升。
?
醫療器械技術評審的安全性有效性都關乎著每一位公民的安全和權益,所以我們一定要做好醫療器械檢測,主要依靠兩種方式,一是找專業的醫療器械檢測機構,二是進行自檢。自檢主要是優勢就是方便,自行購買醫療器械測試儀器,后期可長期進行自行檢查。威夏科技明星產品6%魯爾圓錐接頭多功能測試儀、注射針測試儀、注射器檢測儀器、縫合針測試儀、縫合線檢測設備、輸液器試驗儀 、導管流量測試儀、手術刀片測試儀等等都是中國藥檢、山東威高集團、江蘇魚躍集團、SGS通標、美敦力、邁瑞醫療、協和醫院等研究所、檢驗所、第三方檢測機構、醫療器械耗材生產廠家、醫療機構合作選擇。
?
